
С 23 по 26 июня прошла 83-я научная сессия Американской диабетической ассоциации в гибридном формате. Ключевыми сессиями стали обновление стандартов медицинской помощи ADA 2023, новые терапевтические молекулы в лечении ожирения, а также использование непрерывного мониторинга для пациентов с сахарным диабетом 2-го типа (СД2).
Подробности в нашем обзоре
Американская диабетическая ассоциация выпустила обновления к Стандартам лечения сахарного диабета (СД) 2023 г., касающиеся использования теплизумаба для отсрочки начала сахарного диабета 1-го типа (СД1). Обновления коснулись второй секции под названием «Классификация и диагностика сахарного диабета».
Были выделены 3 стадии развития СД1 (рис. 1).
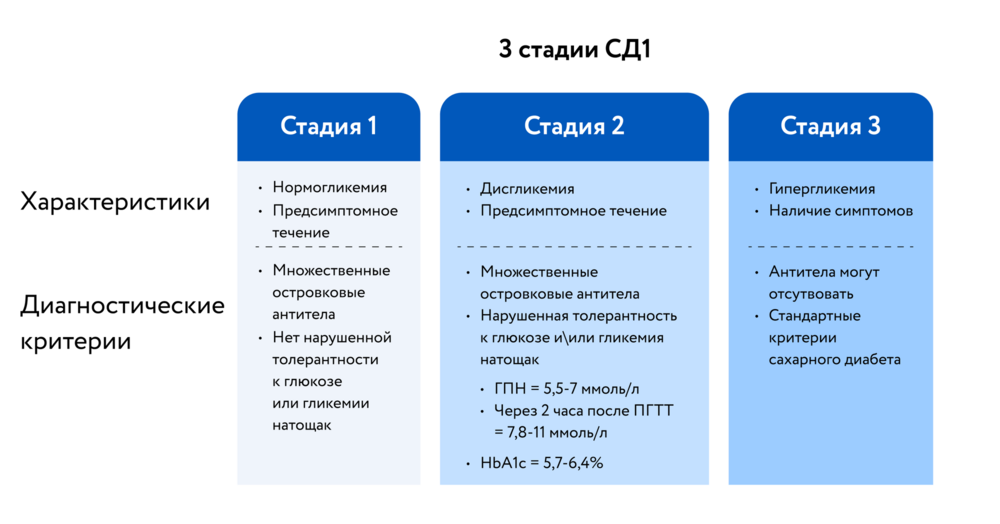
Особое внимание было уделено скринингу пациентов для отсрочки развития СД1 (рис. 2).
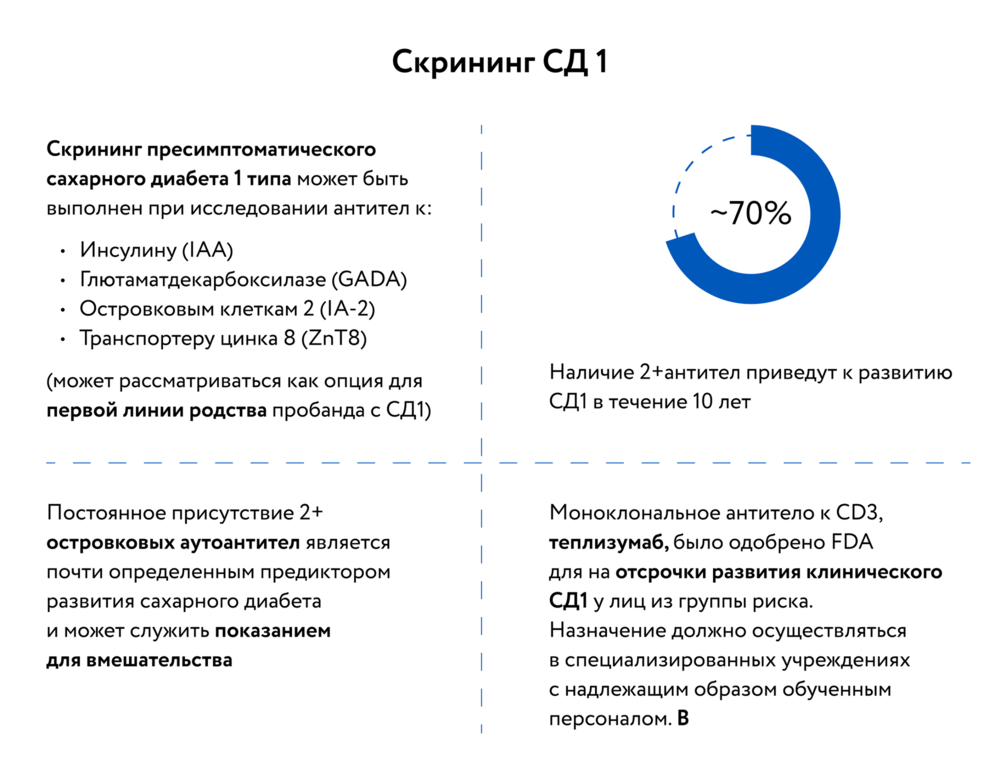
В связи с этим множество сессий были посвящены запущенным программам скрининга и полученным результатам.
1. По данным Американской диабетической ассоциации, это:
2. Примерно у 80% детей и подростков с СД1 первые островковые антитела развиваются в возрасте до 6 лет.
3. Лучшая чувствительность для однократного скрининга — в возрасте 4 лет (40%), для двух скринингов — в возрасте 2 и 6 лет (~ 80%).
На стадии 1:
1. Данные США: более 50% при ДКА St 3, более 80% госпитализированы.
2. ДКА при постановке диагноза предсказывает худший долгосрочный HbA1c, что приводит к долгосрочному риску осложнений.
3. Снижение ДКА, улучшение функции В-клеток на стадии 3, улучшение качества жизни, снижение психологического стресса, плавный переход на инсулинотерапию в нужное время, улучшение отдаленных результатов.
4. ДКА на момент постановки диагноза у детей, прошедших скрининг, менее 5% по сравнению с 62% у детей, не прошедших скрининг*.
5. Скрининг экономически эффективен, если он снижает частоту ДКА на 1/5, т. е. с 50% до 40%, и впоследствии приводит к снижению HBA1c на 1%*.
*Данные на основе программы гибридного аутоимунного скрининга в Колорадо. При скрининге общей популяции (более 33 тысяч детей) распространенность СД1 составила 1%.
1. American Diabetes Association. Diabetes Care 2023;46(Suppl 1):S19-S40.
Конечно же, не была оставлена без внимания тема применения различных препаратов инкретинового ряда. Так, одна из сессий была посвящена эффективности и безопасности применения тирзепатида, двойного агониста рецепторов глюкозозависимого инсулинотропного полипептида (ГИП), и глюкагоноподобного пептида-1 (ГПП-1), вводимого один раз в неделю, — у пациентов с СД и ожирением.
Исследование SURMOUNT-2 представляло собой 72-недельное рандомизированное многоцентровое двойное слепое исследование, целью которого была оценка безопасности и эффективности тирзепатида в дозировках 10 мг и 15 мг в сравнении с плацебо для длительного управления весом у пациентов с СД2 и ожирением.
В исследовании SURMOUNT-2 обе дозировки тирзепатида — 10 мг и 15 мг — продемонстрировали превосходство и клинически значимое снижение массы тела по сравнению с плацебо (первичная конечная точка). Среднее снижение веса через 72 недели составило −13,5 кг и −15,6 кг от исходного, а HbA1c (основная вторичная конечная точка) снизился на 2,14% и 2,22% для 10 мг и 15 мг соответственно. Переносимость и профиль безопасности тирзепатида у пациентов с СД2 и ожирением соответствовали данным исследования SURPASS и других исследований инкретиновых препаратов для лечения ожирения: наиболее часто отмечались НЯ, связанные с ЖКТ (легкой и умеренной тяжести).
Отдельная сессия была посвящена эффективности и безопасности ретатрутида — тройного агониста рецепторов глюкозозависимого инсулинотропного полипептида (ГИП), глюкагоноподобного пептида-1 (ГПП-1) и глюкагона, вводимого один раз в неделю, — при ожирении, НАЖБП и СД2. В ходе исследования фазы 2 у пациентов с ожирением, но без СД при использовании ретатрутида происходило снижение веса на −17,9% при самой высокой дозе 12 мг за 24 недели (первичная конечная точка). Данные за 48 недель были еще более впечатляющими: доза 12 мг привела к снижению веса в среднем на −24,2% (основная вторичная конечная точка). Абсолютное снижение веса составило 26 кг через 48 недель. Пациенты хорошо переносили лечение, а профиль безопасности и переносимости ретатрутида был сопоставим с аналогичными показателями при терапии ГПП-1 и ГИП/ГПП-1.
Согласно данным другого 36-недельного исследования 2-й фазы, при применении ретатрутида у пациентов с СД2 в дозе от 4 до 12 мг по сравнению с плацебо и дулаглутидом в дозе 1,5 мг, уровень HbA1c снизился с 8,3% на исходном уровне до 6,1% на 36-й неделе при дозе 12 мг ретатрутида. При этом 82% участников достигли уровня HbA1c = 6,5% и 31% участников достигли нормогликемии (HbA1c
Таким образом, ретатрутид продемонстрировал значительное улучшение гликемического контроля вплоть до нормогликемии с устойчивым снижением массы тела в масштабах, ранее не показанных ни на одном из препаратов, когда-либо исследовавшихся при СД2.
Широко обсуждались различные аспекты использования устройств для непрерывного мониторирования гликемии у пациентов с СД2 и даже без нарушений углеводного обмена.
В частности, доктор Андерс Карлсон из Университета Торонто, Канада, представил доклад по использованию непрерывного мониторирования гликемии у пациентов с предиабетом и ожирением. Доктор Карлсон начал с актуализации проблемы, а затем привел данные пилотного исследования, включившего 15 пациентов с предиабетом и индексом массы тела более 30 кг/м2, согласно результатам которого использование непрерывного мониторирования гликемии в сочетании с низкоуглеводной диетой выглядит очень перспективным методом управления пищевым поведения, а также хорошо воспринимается пациентами. Подводя итог своему докладу, доктор Карлсон сделал вывод, что непрерывное мониторирование гликемии является перспективным способом профилактики сахарного диабета, который может использоваться в дополнение к диете и физическим упражнениям.
Ронни Аронсон, доктор медицинских наук, рассказал о роли непрерывного мониторирования глюкозы у пациентов с СД2, не получающих терапию инсулином. Лектор подчеркнул, что в настоящее время накоплены убедительные доказательства, подтверждающие влияние ФМГ и НМГ на гликемический контроль у пациентов на инсулинотерапии: с СД1 и СД2 как на ББИТ, так и на базальной инсулинотерапии. Тем не менее ни мониторирование в режиме реального времени, ни флеш-мониторирование не изучались в рамках рандомизированных контролируемых исследований у пациентов с СД2, не использующих инсулин, до момента появления результатов исследования IMMEDIATE. В данном исследовании использование ФМГ приводило к значительному улучшению качества гликемического контроля в виде увеличения времени нахождения в целевом диапазоне на 10%. По словам д-ра Аронсона, популяция пациентов, представленная в данном исследовании, в несколько раз больше, чем популяции, в которых ранее были уже подтверждены преимущества НМГ и ФМГ. Кроме того, это больные с высоким риском осложнений диабета и сердечно-сосудистых исходов. «Терапевтическое обучение в сочетании с НМГ выглядит перспективной опцией для улучшения контроля над диабетом без необходимости добавления еще одного сахароснижающего препарата», — заключил лектор1.
Кроме того, современные технологии позволяют выявлять новые грани применения инновационных опций сахароснижающей терапии. В частности, на данном конгрессе были представлены результаты немецкого проспективного обсервационного исследования CHANCE, включившего 70 пациентов с СД2 и недостаточным гликемическим контролем на терапии БИ+ПССП. Их переводили на фиксированную комбинацию арГПП-1 и БИ (иГларЛикси). Около 30% (n=20) пациентов в данном исследовании применяли флеш-мониторирование глюкозы с оценкой времени в целевом диапазоне (ВЦД), времени выше целевого диапазона (ВВД) и времени ниже целевого диапазона (ВНД) соответственно. Спустя 24 недели терапии иГларЛикси была достигнута тройная цель — 74,5% ВЦД, 22,6% ВВД и 3,5% ВНД, что соответствует целевым значениям показателей по всех актуальных рекомендациях по управлению заболеванием2.
Мы получили Вашу заявку и свяжемся с Вами в ближайшее время для подтверждения регистрации
Укажите адрес почты, использованный при регистрации. Мы отправим вам письмо, которое позволит изменить пароль
Нажимая кнопку «Присоединиться», вы подтверждаете свое согласие на обработку компанией Санофи предоставленных вами в форме персональных данных.
Компания Санофи обязуется соблюдать конфиденциальность отправленных вами сообщений. Адрес электронной почты и иная информация, указанная вами в форме, будет использована исключительно для направления ответа на ваше сообщение.
Компания Санофи не будет использовать указанные вами контактные данные для рассылки не запрашиваемых материалов и информации.
Мы получили Вашу заявку и свяжемся с Вами в ближайшее время для подтверждения регистрации
Обращаем Ваше внимание на то, что процесс регистрации не был завершен! Для завершения регистрации Вам необходимо подписать согласие на обработку персональных данных. После этого Вам будут доступны все ресурсы нашего сайта.

Подтвердите свои данные для возобновления доступа. Для этого введите код, отправленный на указанный контакт, и подтвердите сведения о себе.

Вы покидаете ресурс Санофи и переходите на сторонний сайт.
Компания Санофи не несет ответственности за содержание материалов,
размещенных на стороннем ресурсе.
Ссылка:
Подтвердите переход нажатием на кнопку «Перейти» или «Отменить»
